Η εναλλακτική συρραφή του RNA είναι κάτι σαν το μοντάζ των ταινιών. Ο δημιουργός, μπορεί να δημιουργήσει διαφορετικές εκδοχές της ταινίας του, απλά κόβοντας και τοποθετώντας τις σκηνές που επιθυμείς. Κάπως έτσι, και τα κύτταρά μας συρράπτουν το RNA με διαφορετικούς τρόπους, ώστε να παράγουν μια ποικιλία πρωτεϊνών, από το ίδιο γονίδιο, κάτι που ρυθμίζει την λειτουργία τους ανάλογα με τις ανάγκες του οργανισμού. Ο καρκίνος είναι το αποτέλεσμα όταν αυτή η διαδικασία δε δουλεύει όπως θα έπρεπε, κάτι που δημιουργεί και αναπτύσσει έναν όγκο.
Μια νέα μελέτη όμως δημοσιεύθηκε στο τεύχος του Nature Communications, στις 15 Φεβρουαρίου, από τους επιστήμονες στο Jackson Laboratory (JAX) και το UConn Health. Σε αυτή διαβάζουμε πως ο καρκίνος παραβιάζει αυτή τη διαδικασία συρραφής του RNA, αλλά από την άλλη, με την ίδια διαδικασία μπορεί να δοθεί θεραπεία που θα επιβραδύνει ή και θα συρρικνώσει επιθετικούς και δύσκολα ιάσιμους όγκους.
Με αυτό τον τρόπο, ίσως σύντομα αποκτήσουμε τα μέσα για να αντιμετωπίσουμε επιθετικούς καρκίνους, όπως ο καρκίνος στον εγκέφαλο ή ο καρκίνος του μαστού. Σε αυτές τις περιπτώσεις, η μέχρι σήμερα λύσεις είναι αρκετά περιορισμένες και αυτή η μέθοδος ίσως φέρει επανάσταση.
Στο επίκεντρο αυτής της εργασίας, με επικεφαλής την Olga Anczuków, αναπληρώτρια καθηγήτρια στο JAX και επικεφαλής προγράμματος στο JAX Cancer Center που έχει οριστεί από το NCI, βρίσκονται μικροσκοπικά γενετικά στοιχεία που ονομάζονται εξόνια δηλητηρίου (poison exons), ο «διακόπτης απενεργοποίησης(kill switch)» της ίδιας της φύσης για την παραγωγή πρωτεΐνης. Όταν τα εξόνια υπάρχουν σε ένα μήνυμα RNA, προκαλούν την καταστροφή του πριν καταφέρει να δημιουργήσει την πρωτεΐνη, σταματώντας έτσι την επιβλαβή κυτταρική δραστηριότητα.
Στην περίπτωση των υγιών κυττάρων, τα εξόνια ρυθμίζουν τα επίπεδα των βασικών πρωτεϊνών στον οργανισμό μας, διατηρώντας τον γενετικό μηχανισμό υπό έλεγχο. Στην περίπτωση του καρκίνου όμως, αυτός ο μηχανισμός υπολειτουργεί και παράγει πρωτεΐνες που δεν πρέπει, δημιουργώντας τους όγκους.
Η Anczuków και η ομάδα της, συμπεριλαμβανομένου του Nathan Leclair, MD/Ph.D. μεταπτυχιακός φοιτητής στο UConn Health and The Jackson Laboratory που πρωτοστάτησε στην έρευνα, και ο Mattia Brugiolo, ερευνητής του προσωπικού που συνεισέφερε την τεχνογνωσία του, ανακάλυψαν ότι τα καρκινικά κύτταρα καταστέλλουν τη δραστηριότητα των εξονίων δηλητηρίου σε ένα κρίσιμο γονίδιο που ονομάζεται TRA2β. Ως εκ τούτου, τα επίπεδα της πρωτεΐνης TRA2β αυξάνονται μέσα στα καρκινικά κύτταρα, προκαλώντας πολλαπλασιασμό του όγκου.
Παράλληλα, η ομάδα βρήκε μια συσχέτιση μεταξύ των επιπέδων των εξονίων δηλητηρίου και των αποτελεσμάτων των ασθενών. «Δείξαμε για πρώτη φορά ότι τα χαμηλά επίπεδα συμπερίληψης εξονίων δηλητηρίου στο γονίδιο TRA2β σχετίζονται με κακή έκβαση σε πολλούς διαφορετικούς τύπους καρκίνου, και ειδικά σε επιθετικούς και δύσκολα αντιμετωπίσιμους καρκίνους», δήλωσε η Anczuków. Αυτά περιλαμβάνουν τον καρκίνο του μαστού , τους όγκους του εγκεφάλου, τους καρκίνους των ωοθηκών , τους καρκίνους του δέρματος, τις λευχαιμίες και τους καρκίνους του παχέος εντέρου , εξήγησε η Anczuków.
Οι επιστήμονες της ομάδας προσπάθησαν στη συνέχεια να αυξήσουν τη συμπερίληψη του εν λόγω εξονίου στο γονίδιο TRA2β και κατάφεραν να ενεργοποιήσουν ξανά το kill switch. Βρήκαν την απάντησή τους στα αντιπληροφοριακά ολιγονουκλεοτίδια (ASOs) – συνθετικά θραύσματα RNA που μπορούν να σχεδιαστούν για να αυξάνουν την συμπερίληψη εξονίων δηλητηρίου με συγκεκριμένους τρόπους. Όταν εισήχθησαν στα καρκινικά κύτταρα, τα ASOs ουσιαστικά ανέτρεψαν τον γενετικό διακόπτη, αποκαθιστώντας τη φυσική ικανότητα του σώματος να υποβαθμίζει την περίσσεια του TRA2β RNA και να αναστέλλει την εξέλιξη του όγκου.
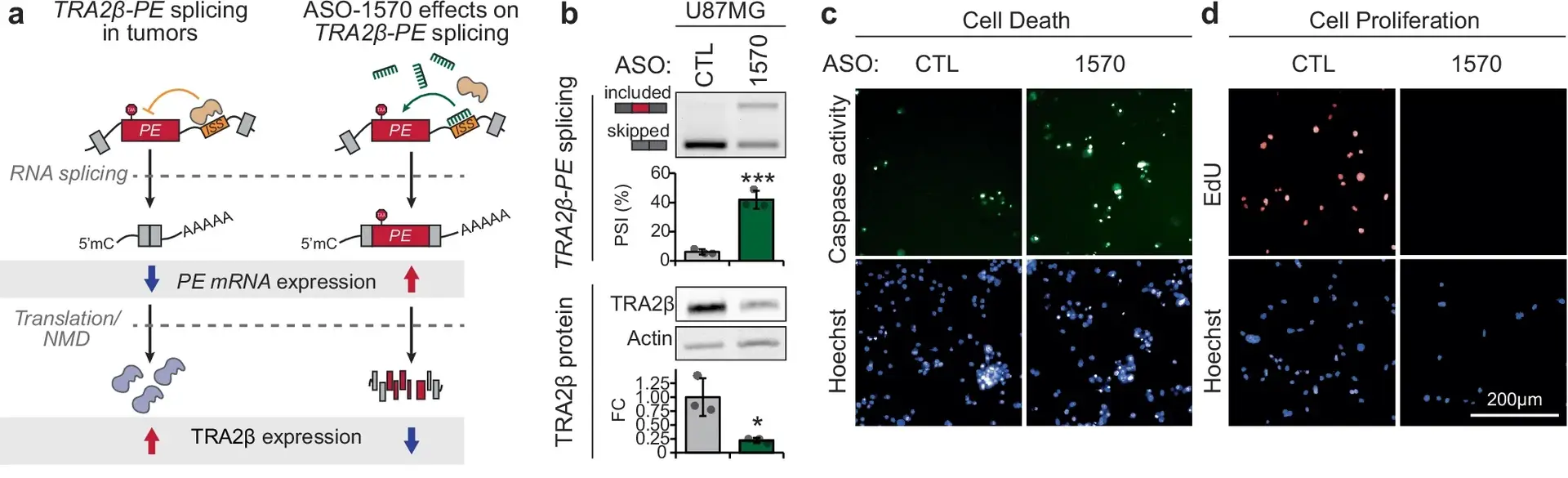
«Διαπιστώσαμε ότι τα ASO μπορούν να ενισχύσουν γρήγορα την συμπερίληψη των εξονίων δηλητηρίου, ξεγελώντας ουσιαστικά το καρκινικό κύτταρο ώστε να απενεργοποιήσει τα δικά του σήματα ανάπτυξης», είπε ο Leclair. «Αυτά τα δηλητηριώδη εξόνια λειτουργούν σαν ρεοστάτης, προσαρμόζοντας γρήγορα τα επίπεδα πρωτεΐνης – και αυτό θα μπορούσε να κάνει τα ASO μια εξαιρετικά ακριβή και αποτελεσματική θεραπεία για επιθετικούς καρκίνους».
GPS χωρίς σήμα – Αλλάζει ο τρόπος σε υπηρεσίες γεωεντοπισμού
Είναι ενδιαφέρον ότι όταν οι ερευνητές αφαίρεσαν πλήρως τις πρωτεΐνες TRA2β χρησιμοποιώντας επεξεργασία γονιδίων CRISPR, οι όγκοι συνέχισαν να αναπτύσσονται – υποδηλώνοντας ότι η στόχευση του RNA αντί της πρωτεΐνης θα μπορούσε να είναι μια πιο αποτελεσματική προσέγγιση. «Αυτό μας λέει ότι το RNA που περιέχει δηλητήριο δεν σιωπά απλώς το TRA2β», εξήγησε ο Anczuków. «Πιθανότατα δεσμεύει άλλες πρωτεΐνες που κολλούν στο RNA, δημιουργώντας ένα ακόμη πιο τοξικό περιβάλλον για τα καρκινικά κύτταρα».
Φυσικά χρειάζονται περισσότερες μελέτες για να βελτιωθούν οι θεραπείες που βασίζονται στο ASO, αλλά και τους τρόπους παράδοσης του στου όγκους. Όμως, τα πρώτα αποτελέσματα δείχνουν πως τα ASO χτυπούν πολύ συγκεκριμένα τα καρκινικά κύτταρα και δεν παρεμβαίνουν στη φυσιολογική κυτταρική λειτουργία, κάτι που τα καθιστά πολλά υποσχόμενα στις μελλοντικές θεραπείες κατά του καρκίνου!
Η μελέτη δημοσιεύθηκε στο Nature Communications.
Ακολουθήστε το Techmaniacs.gr στο Google News για να διαβάζετε πρώτοι όλα τα τεχνολογικά νέα. Ένας ακόμα τρόπος να μαθαίνετε τα πάντα πρώτοι είναι να προσθέσετε το Techmaniacs.gr στον RSS feeder σας χρησιμοποιώντας τον σύνδεσμο: https://techmaniacs.gr/feed/.


























![Samsung Galaxy S26 Ultra Review: Είναι τελικά Ultra; [Βίντεο] Galaxy S26 ultra review](https://techmaniacs.gr/wp-content/uploads/2026/03/Galaxy-S26-ultra-review-218x150.webp)