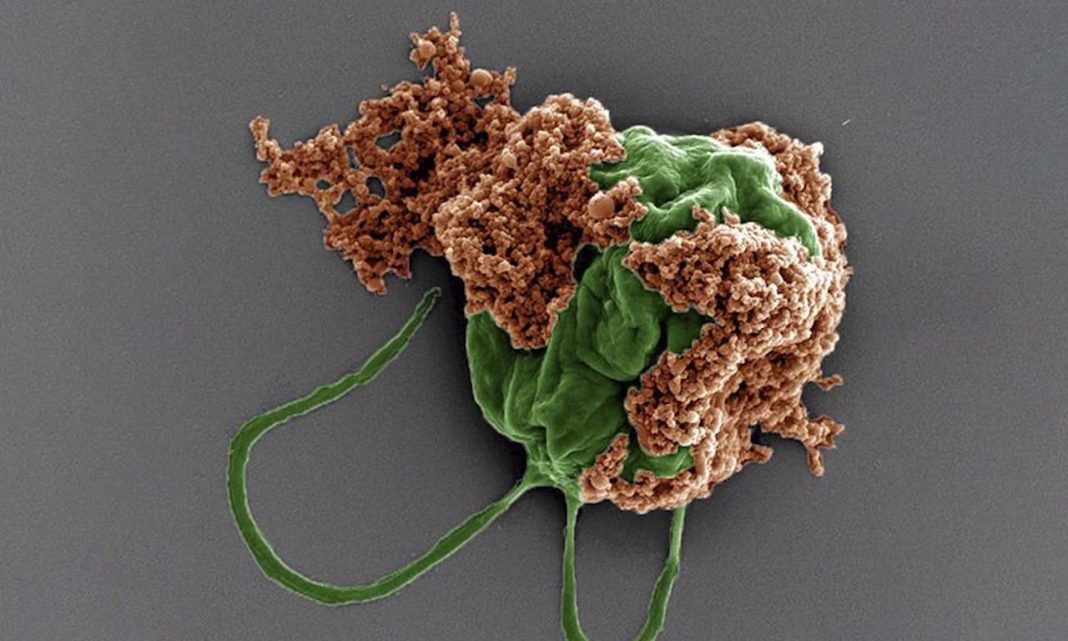
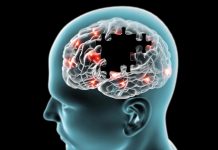
Μια ομάδα επιστημόνων του Πανεπιστημίου της Μασαχουσέτης προέβη στην ανάπτυξη μιας μη τοξικής βακτηριακής θεραπείας, γνωστής ως BacID για την διοχέτευση αντικαρκινικών φαρμάκων απευθείας στους όγκους. Η τεχνολογία υπόσχεται πολύ ασφαλή και αποτελεσματικότερη θεραπεία καρκίνων με υψηλά ποσοστά θνησιμότητας, συμπεριλαμβανομένων του καρκίνου του ήπατος, των ωοθηκών και του μεταστατικού καρκίνου του μαστού.
Οι κλινικές δοκιμές αναμένεται να ξεκινήσουν το 2026. Αυτό που προσπαθούμε να κάνουμε είναι να ξεκλειδώσουμε τη δυνατότητα να θεραπεύσουμε καρκίνους σε προχωρημένο στάδιο, αναφέρουν οι συγγραφείς της μελέτης. Τα βακτήρια κατοικούν φυσικά στους όγκους και επειδή αυτή η θεραπεία είναι τόσο στοχευμένη, μπορεί να θεραπεύσει ορισμένους καρκίνους χωρίς τις παρενέργειες που θα βλέπατε με άλλες συστηματικά χορηγούμενες θεραπείες, όπως η χημειοθεραπεία.
Κάνε απαραβίαστο το Gmail και τον Google λογαριασμό απλά με αυτή τη ρύθμιση
Πιο συγκεκριμένα, η ομάδα έχει προβεί στην ανάπτυξη μη τοξικών, γενετικά τροποποιημένων στελεχών σαλμονέλας που στοχεύουν τους όγκους και στη συνέχεια ελέγχουν την απελευθέρωση φαρμάκων που καταπολεμούν τον καρκίνο στο εσωτερικό των καρκινικών κυττάρων. Εκτός από το ότι γλιτώνει τους υγιείς ιστούς από βλάβες, αυτή η θεραπεία συνεχίζει να δρα και μετά την χορήγηση του φαρμάκου και για μεγάλο διάστημα, επειδή τα βακτήρια αναπτύσσονται εκθετικά στους όγκους.
Οι επιστήμονες προσπάθησαν να κάνουν το στέλεχος όσο πιο ασφαλές και φιλικό για τον χρήστη. Παράλληλα πέτυχαν να ελέγχουν πότε τα βακτήρια, μετά την ενδοφλέβια έγχυση, εισβάλλουν στα καρκινικά κύτταρα και παρέχουν τη θεραπεία. Αυτό βελτίωσε σημαντικά την ικανότητα στόχευσης των όγκων με υψηλότερες συγκεντρώσεις της φαρμακευτικής θεραπείας, ενώ παράλληλα έκανε τη θεραπεία πολύ πιο ασφαλή.
«Στο στέλεχος πρώτης γενιάς, ουσιαστικά βασιζόμασταν στον ίδιο τον εγκέφαλο του βακτηρίου για να βρει τον όγκο και να παραδώσει τη θεραπεία. Αλλά δεν μπορούσαμε να ελέγξουμε ακριβώς πότε συνέβαινε αυτό, οπότε υπήρχαν κίνδυνοι που σχετίζονταν με την εισβολή σε υγιή κύτταρα, καθώς και με την πρόωρη απομάκρυνση των βακτηρίων πριν αποικίσουν τους όγκους, και θέλαμε να μετριάσουμε και τους δύο κινδύνους» εξηγούν οι επιστήμονες.
Επανεγγραφή στο taxisnet για όλους αυτούς τους πολίτες χωρίς κλειδάριθμο
Η ερευνητική ομάδα ανακάλυψε ότι το «μαστίγιο» των βακτηρίων (η μικρή «ουρά» που προεξέχει από τα βακτήρια και τα βοηθά να κινούνται) είναι εκείνο που τους επιτρέπει να εισέρχονται στα καρκινικά κύτταρα. Έτσι δημιούργησαν ένα γενετικό κύκλωμα στα βακτήρια το οποίο οδηγεί στην παραγωγή «μαστιγίων» με χρήση μιας μικρής δόσης… ασπιρίνης. Χωρίς αυτόν τον «διακόπτη» που παρέχει το σαλικυλικό οξύ (το ενεργό συστατικό της ασπιρίνης), τα βακτήρια παραμένουν σε «ύπνωση» μέσα στους όγκους.
«Το πρώτο ζωτικής σημασίας τμήμα αυτής της τεχνολογίας είναι η ελεγχόμενη ενεργοποίηση των μαστιγίων» εξήγησε ο δρ Ράμαν και συμπλήρωσε ότι «το άλλο ζωτικής σημασίας τμήμα της τεχνολογίας μας αφορά το κύκλωμα ‘αυτοκτονίας’ των βακτηρίων που αναπτύξαμε αφού τα βακτήρια έχουν πλέον εισέλθει στα καρκινικά κύτταρα. Καθώς τα βακτήρια ‘αυτοκτονούν’ εκλύουν τη θεραπεία μέσα στα καρκινικά κύτταρα».
με πληροφορίες από in.gr και το βήμα
Ακολουθήστε το Techmaniacs.gr στο Google News για να διαβάζετε πρώτοι όλα τα τεχνολογικά νέα. Ένας ακόμα τρόπος να μαθαίνετε τα πάντα πρώτοι είναι να προσθέσετε το Techmaniacs.gr στον RSS feeder σας χρησιμοποιώντας τον σύνδεσμο: https://techmaniacs.gr/feed/.

![[Αποκλειστικό] H Samsung θα αυξήσει τις τιμές των κινητών της τον Ιούνιο Samsung Galaxy S27 Pro Mobile αύξηση τιμές](https://techmaniacs.gr/wp-content/uploads/2026/03/galaxy-s26-ultra-17-218x150.webp)



























![Samsung Galaxy S26 Ultra Review: Είναι τελικά Ultra; [Βίντεο] Galaxy S26 ultra review](https://techmaniacs.gr/wp-content/uploads/2026/03/Galaxy-S26-ultra-review-218x150.webp)